장애인 환자의 치과진료에서 레미마졸람의 이해와 임상적 적용: 문헌고찰
Understanding and clinical application of remimazolam in dental treatment for patients with special needs: A literature review
Article information
Trans Abstract
Patients with intellectual disability, autism spectrum disorder, cerebral palsy, or severe dental fear often have difficulty undergoing routine outpatient dental treatment, leading to repeated delays or treatment failure. In such cases, sedation may serve as an important option bridging general anesthesia and routine outpatient care. Remimazolam is a recently introduced sedative and general anesthetic agent approved in major regions. This article reviews the clinical significance of remimazolam in dental treatment for patients with disabilities and summarizes the rationale for considering it as an agent for dental sedation.
서론
지적장애, 자폐스펙트럼장애, 뇌병변장애가 있거나 치과 공포가 매우 심한 환자는 일반적인 외래 치료가 어려워 진료가 반복적으로 실패하거나 지연된다. 따라서 장애인 치과진료에서는 단순히 치료의 술식적 난이도에만 주목하기보다, 어떤 방식으로 접근해야 환자에게 가장 안전하고 지속 가능한 치료 경험을 제공할 수 있는가를 함께 고민해야 한다. 이러한 맥락에서 진정마취는 전 마취와 일반 외래 치료 사이를 잇는 중요한 선택지가 될 수 있다 .
최근 주목받고 있는 레미마졸람(remimazolam)은 프로포폴(propofol) 허가 이후 약 30여 년 만에 등장한 새로운 진정·전신마취 약제로, 일본(2020), 미국(2020), 중국(2020), 유럽(2021), 한국(2021) 등 주요 국가에서 사용 승인을 받았다[1,2]. 특히 미국 FDA의 NDA 임상심사 문서에서 시술진정(procedural sedation) 시 비마취과 진료자(non-anesthesia providers)가 사용할 수 있는 진정제로 언급된 바 있어, 치과 진정마취 영역에서도 시사하는 바가 크다[3].
그러나 진정마취 약제는 익숙하게 사용될수록, 오히려 그 작용 원리와 한계를 충분히 이해하지 못한 채 반복적으로 사용되기 쉽다. 이에 본 글에서는 장애인환자의 치과 치료라는 임상적 맥락 속에서 레미마졸람(remimazolam)의 의미를 살펴보고, 치과진정마취 약제로 고려할 수 있는 근거에 대해 정리해 보고자 한다.
본론
레미마졸람의 약리학적 특성과 임상적 장점
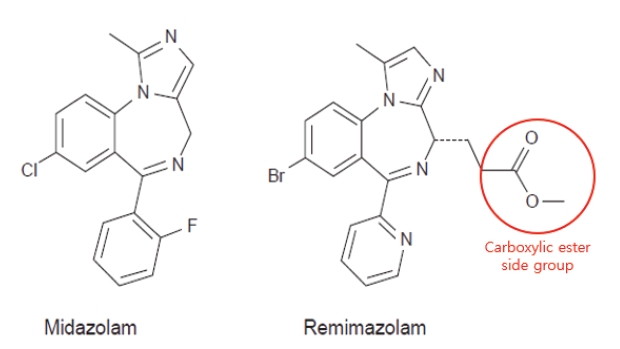
이하에서는 치과 진정에서 흔히 사용되는 미다졸람과 시술 진정에서 널리 사용되는 프로포폴과의 비교를 통해 레미마졸람(Fig. 1)의 특성을 살펴보고자 한다.
1. 빠른 작용 발현과 빠른 회복
1) 빠른 작용 발현(rapid onset)
벤조다이아제핀(benzodiazepine) 계열의 약물: 양성알로스테릭조절자(positive allosteric modulator)로써의 역할
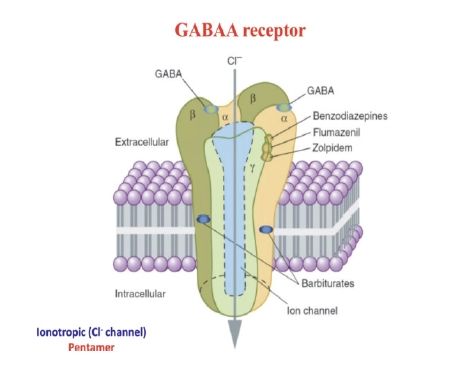
뇌의 신경활동은 흥분시스템과 억제시스템의 균형으로 작동한다. 그 중 억제시스템은 GABA-A receptor(Fig. 2)에 의해 작용한다. 글루탐산(glutamate)에 의해 생성된 GABA(γ-aminobutyric acid)는 GABA-A 수용체의 α–β interface 에 결합해 Cl- 채널을 개방하여 신경 흥분성을 낮추는 역할을 한다. 이때 투약된 벤조디아제핀은 GABA-A 수용체의 α–γ interface 결합하여 양성 알로스테릭 조절자로 기능한다. 즉, GABA에 의한 Cl- 채널 개방 빈도를 증가시켜 과분극을 유도해 진정, 불안 감소, 경련 억제 같은 효과를 나타낸다. 이러한 이유로 벤조다이아제핀 계열은 진정마취를 위해 사용된다[3].
2) 빠른 회복(rapid recovery)
레미마졸람의 특징적인 화학구조를 통해 초단기간작용(ultra-short acting)의 원인을 찾을 수 있다.
2. 에스터 측쇄(carboxylic ester side group)(Fig. 3)
미다졸람의 화학 구조에 에스터 측쇄의 도입[4,5]으로 미다졸람보다 반감기가 짧아 인지 기능의 빠른 회복이 가능하다[6-9].
3. 장기 비의존성 대사(organ-independent metabolism)
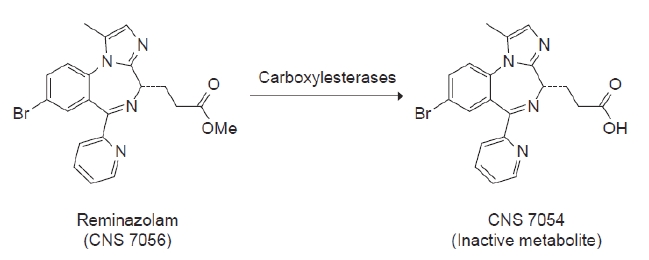
대부분 혈장의 에스터라아제(esterase)에 의해서 빠르게 가수분해되며, 비활성 카복실산 대사산물인 CNS7054로 전환된다[5,9,10](Fig. 4). 즉, 이 약물은 미다졸람처럼 CYP450 매개 대사와 같은 cytochrome 의존성 간 대사 경로에 주로 의존하지 않기 때문에, 임상적으로 유의한 약물대사 상호작용의 가능성이 상대적으로 낮다[11].
4. 비활성 대사체(inactive metabolite): CNS7054
장기 비의존성 대사를 통해 레미마졸람으로부터 비활성 대사체는 CNS7054이다. 이 물질은 벤조다이아제핀 결합부위에 다시 붙어 작용하는 미다졸람의 활성대사체인 α-hydroxymidazolam과 달리 벤조다이아제핀 결합부위 친화도가 약 50배 정도 더 낮고[5,12], 약 99.7%가 소변으로 배설된다[14]. 또한 CNS7054는 원약물 레미마졸람에 비해 GABA_A 수용체에 대한 친화도가 최소 300배 이상 낮아 약리학적 활성이 거의 없다[7,13].
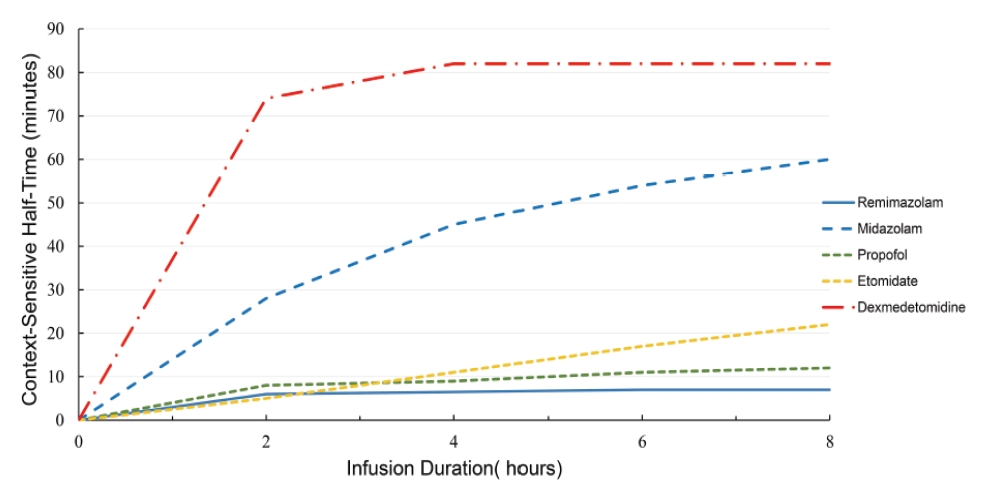
이러한 대사 및 배설 특성은 레미마졸람의 상황민감성반감기가 작은(Fig. 5) 것을 의미하고 초단시간 작용과 비교적 예측 가능한 회복 양상을 설명하는 중요한 근거가 된다[15].
5. 레미마졸람의 용량-의존적인 특성에 대한 연구결과
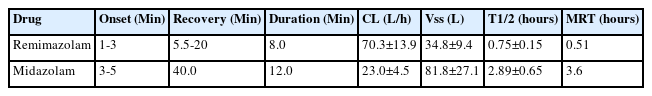
건강한 지원자를 대상으로 한 제1상 약동학 및 약력학 연구에서, 레미마졸람은 0.05 mg/kg부터 빠른 진정 유도(rapidonset sedation)가 관찰되었고, 0.075 mg/kg 이상에서는 주사 후 1–2분 이내에 최대 진정 효과(peak sedation effect)에 도달하였다[16]. 또한 0.075–0.2 mg/kg 범위에서는 미다졸람 0.075 mg/kg보다 더 큰 진정 효과를 보이면서도 회복 시간은 더 짧게 유지되었다. 실제로 진정 지속(duration of sedation) 시간과 완전 각성(full alert)까지의 중앙시간(median time)은 각각 8분 대 12분, 5.5–20분 대 40분으로 보고되었다[7,16].
같은 연구에서 레미마졸람의 전신 청소율(systemic clearance, CL)은 미다졸람보다 약 3배 높았고[(70.3±13.9) L/h vs (23.0±4.5) L/h], 정상상태 분포용적(steady-state volume of distribution, Vss)은 약 50% 수준이었으며[(34.8±9.4) L vs (81.8±27.1) L], 말기 반감기(terminal half-life, T1/2) 역시 더 짧았다(0.75±0.15시간 vs 2.89±0.65시간) [7]. 그 결과 평균체류시간(mean retention time)은 미다졸람의 약 1/7 수준(0.51시간 vs 3.6시간)이었다[7](Table 1). 또한 2020년 시행한 지속 주입(continuous infusion) 연구에서는 4시간 주입 후 상황민감성감소시간(context-sensitive decrement time)이 6.8±2.4분으로 짧았고, 주입 중단 후 완전 각성까지의 시간도 19±7분으로 보고되어[10], 레미마졸람이 지속 주입 상황에서도 비교적 빠르고 예측 가능한 회복 특성을 가진다는 점을 뒷받침하였다.
6. 비교적 안정적인 혈역학적 특성
1) 혈역학적 안정성에 대한 연구 결과
연구에 따르면 레미마졸람은 PR 간격, QRS duration, QTcI(individually corrected QT)에 임상적으로 유의한 변화를 보이지 않았고, 심박수(Heart Rate), 혈압(BP), 호흡수(Respiratory rate)에도 큰 영향을 주지 않았다[7,10].
또한 양을 대상으로 한 전임상 연구에서는 뇌의 폭발-억제 패턴(burst suppression pattern)이나 등전위뇌파(isoelectric EEG)가 관찰되지 않았으며, 수술 후 인지기능장애 발생 또한 감소하는 것으로 보고되었다. 이러한 소견은 레미마졸람이 신경학적 기능 회복에 유리하게 작용할 가능성을 뒷받침한다[17-19].
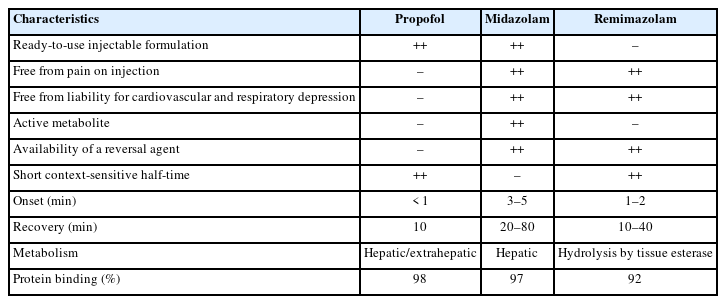
2) 미다졸람 vs 레미마졸람(Table 2)
미다졸람은 치과진정치료에서 가장 흔히 사용되던 벤조다이아제핀계열 약물로써 작용 발현이 3–5분이지만, 상황민감성반 감기가 길다. 또한 미다졸람은 활성대사산물이 잔효에 영향을 줄 수 있어, 장시간 주입이나 고령, 간기능 저하, 약물상호작용 등의 상황에서는 회복이 지연될 수 있다[20].
미다졸람을 투여 받은 환자들과 비교했을 때, 레미마졸람을 투여 받은 경우 저혈압(hypotension)을 경험한 환자가 더 적었고 회복도 더 빨랐으며, 혈압 변동(blood pressure perturbation)과 호흡억제(respiratory depression)의 위험도 낮았다[21-24]. 이러한 결과는 레미마졸람이 미다졸람과 비교했을 때, 시술진정을 위해 안전하게 투여될 수 있음을 시사한다.
3) 프로포폴 vs 레미마졸람(Table 2)
프로포폴은 시술진정에서 가장 흔히 사용되는 정맥마취제로, 작용 발현이 빠르며 15~40초[25] 반감기가 매우 짧아 각성이 빠르고 인지 기능 회복도 신속하다. 하지만 주사 시 통증이 있고, 플루마제닐(flumazenil)과 같은 길항제가 없기 때문에 프로포폴 사용 시 유효성을 유지하면서도 더 안전한 진정제에 대한 필요성이 요구된다[3].
한편 레미마졸람군과 프로포폴군을 비교한 연구에서는, 저혈압 발생률(각각 13.0% vs 42.9%)과 호흡억제 발생률(각각 1.1% vs 6.9%)이 레미마졸람군에서 유의하게 낮게 나타났다[3]. 특히 프로포폴군에서는 고령의 환자에서 저혈압과 심혈관 억제, 호흡억제, 서맥(bradycardia) 등의 이상반응이 더 발생했다[26].
즉, 레미마졸람과 프로포폴은 진정 성공률은 유사하였지만, 레미마졸람이 프로포폴보다 더 우호적인 혈역학적 안전성을 보였다[27].
7. 플루마제닐로 역전 가능한 레미마졸람
이미 정맥로가 확보 되어 있는 상황에서 역전 가능한 길항제가 존재한다는 점과, 미다졸람의 단점 중 하나인 재진정(resedation) 이 일어나지 않는다[28]는 점은 외래 진정에서의 회복을 예측하는 데 큰 역할을 한다.
장애인 환자 치과 치료에서의 레미마졸람의 임상적 의미
진정마취(dental sedation)는 협조도 저하 환자에서 매우 중요한 전략적 의미를 가진다. 환자의 불안과 긴장을 낮추고, 치과 치료 자극에 대한 과도한 반응을 완화함으로써 외래 진료의 가능성을 높일 수 있다[29-31].
1. 전신마취와 외래치료 사이의 가교역할
장애인환자 치과 진료 시, 일반 외래 치료가 어렵다고 해서 곧바로 전신마취로 넘어가야 하는 것은 아니다. 외래 치료는 어렵지만, 전신마취까지 필요하다고 보기에는 과한 경우 외래 진정치료를 시행할 수 있다.
레미마졸람은 비교적 빠른 발현과 회복 등의 장점을 근거로 짧은 외래 처치나 반복적인 유지 관리 치료 및 예방적 관리를 가능하게 하여, 증상이 악화된 뒤에야 내원하는 상황을 줄이는 데 도움이 될 수 있다.
2. 반복적인 치료 실패와 부담 완화 가능성
장애인환자의 치과 진료가 어려운 이유는 단순히 치료가 복잡해서만은 아니다. 진료실에서의 치료 실패 경험이 누적되면, 환자 본인은 물론 보호자와 의료진 모두에게 상당한 심리적·신체적 부담이 쌓이게 된다. 적절한 환자 선택 하에 레미마졸람을 이용한 진정이 성공적으로 이루어진다면, 치료 중 갑작스러운 저항이나 중단 가능성을 줄이고 술식을 보다 안정적으로 마무리할 수 있다. 이는 치료 경험을 보다 예측 가능하게 만들고, 반복적인 내원과 실패로 인한 피로를 줄이는 데 기여할 수 있다.
레미마졸람의 한계와 임상적 고려사항
1. 레미마졸람은 진정제이지 근이완제는 아니다.
레미마졸람은 진정 효과를 유도할 수 있으나, 근이완 효과를 기대할 수 있는 약물은 아니다. 따라서 근이완제를 별도로 사용하지 않는 경우 혀의 움직임이나 구강 주위의 불수의적 움직임을 완전히 배제하기 어렵다.
2. 불수의운동·방어반응·공포감이 큰 환자에서는 한계가 있다.
불수의적 움직임이 매우 심한 뇌병변 환자나 방어 행동이 강한 환자, 공포감이 매우 큰 경우, 기대한 수준의 진정 효과가 충분히 얻어지지 않을 수 있다. 이러한 환자에서는 무리하게 외래 진정을 반복하기보다, 상급병원 의뢰를 통한 전신마취가 더 적절한 선택이 될 수 있다.
3. 길항제가 있어도 안전이 자동 보장되는 것은 아니다.
레미마졸람은 플루마제닐로 역전이 가능하지만 길항제의 존재가 안전을 담보하지는 않으므로 적절한 모니터링과 기도관리, 응급대응 체계를 전제로 해야 한다. 특히 경련이 심한 환자에서 아티반(Ativan) 등의 벤조디아제핀 계열 약물을 이미 경구 복용하고 있는 경우, 플루마제닐이 기존 약물의 항경련 효과까지 약화시킬 가능성을 고려해야 하므로 관련 진료과와의 사전 협의가 중요하다.
4. 환자 상태에 따라 용량 조절과 신중한 접근이 필요하다.
1) 신기능 저하 환자
레미마졸람은 건강한 사람과 말기 신질환 환자 사이에서 약동학적 차이가 크지 않아 신기능 저하 환자에서도 용량 조절 없이 사용할 수 있는 것으로 보고되었다[32,33].
2) 간기능 저하 환자
반면 중증 간기능 저하 환자(Child-Pugh 점수 ≥10)에서는 곡선하면적(AUC), 정상상태분포용적(Vss), 반감기, 회복 시간이 증가하므로 마취 또는 진정 유지 시 보다 신중한 접근이 필요하다[1,33].
3) 고령의 환자
또한 Chae et al. 등은 연령이 높아질수록 ED95(Effective Dose 95)가 감소하므로 투여 용량을 감소하도록 제시하였다.
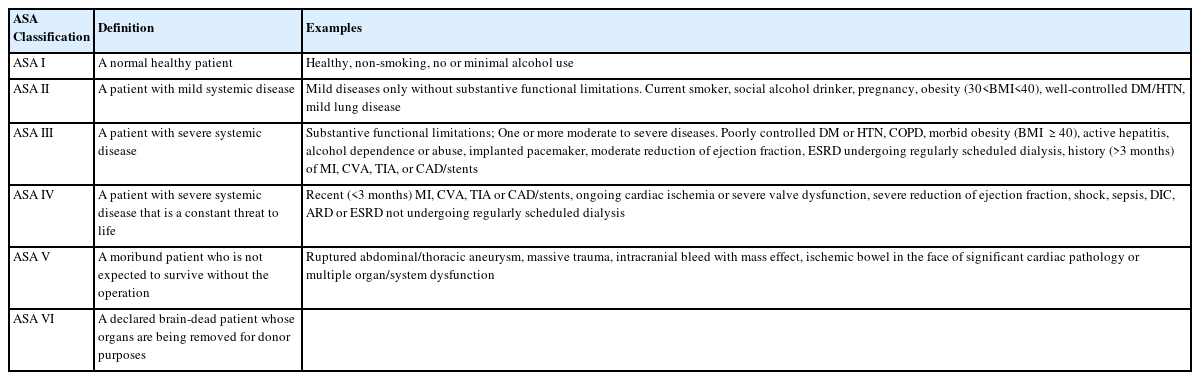
4) ASA 분류에 따른 용량 조절(Table 3)
레미마졸람의 약동학은 연령, ASA class, 성별, 인종의 영향을 크게 받지 않는 것으로 알려져 있으나, 허약한 고령자나 ASA class 3 이상 환자에서는 더 낮은 주입 용량을 고려하는 것이 바람직하다[1,34].
5) 이상반응과 허가사항 변경에 대한 인지도 필요
레미마졸람은 비교적 안정적인 약제로 평가되지만, 이상반응 가능성을 간과해서는 안 된다. 2022년 12월 15일 식품의약품안전처는 시판 후 보고를 반영하여 빈도불명의 아나필락시스(anaphylaxis) 반응을 이상반응 항목에 추가하였다. 따라서 실제 진료 시 허가사항상 주의점과 이상반응에 대한 인지도 함께 갖추는 것이 필요하다.
결론
레미마졸람은 초단시간 작용, 비교적 예측 가능한 회복, 그리고 플루마제닐을 통한 역전 가능성을 바탕으로 치과 진정마취 영역에서 주목할 만한 선택지로 자리매김하고 있다. 특히 협조도 저하로 인해 일반 외래 진료가 어려운 장애인환자에서, 외래 치료와 전신마취 사이의 간극을 메우는 현실적인 중간 단계의 전략이 될 수 있다는 점에서 임상적 의미가 크다. 또한 정기 검진과 예방적 처치의 접근성을 높이고, 반복적인 치료 실패와 그에 따른 보호자 및 의료진의 부담을 줄일 수 있다는 점에서 도 중요한 의의를 가진다.
그러나 레미마졸람은 어디까지나 진정제이며, 모든 장애인 환자에서 동일한 효과를 기대할 수 있는 만능의 해법은 아니다. 환자의 협조도, 불수의운동, 기도 위험, 치료의 침습도와 시간, 전신상태 등을 종합적으로 평가하여 적절한 적응증을 선정하는 것이 무엇보다 중요하다. 아울러 진정치료는 충분한 사전 평가와 모니터링, 응급상황 대응 체계를 전제로 이루어져야 하며, 고령자나 특정 고위험 환자군에서는 더욱 신중한 접근이 필요하다. 식품의약품안전처의 의료용 마약류 마취제 안전사용 기준에서도 고령자에서는 투여량 및 투여속도 조절의 필요성을 제시하고 있으며, 만 18세 미만 소아에 대해서는 안전성·유효성이 확립되어 있지 않다고 명시하고 있다.
결국 장애인 치과진료에서 레미마졸람의 가치는 약물 자체의 우수성에만 있는 것이 아니라, 환자 특성을 고려한 보다 안전하고 지속가능한 치료를 가능하게 한다는 점에서 평가되어야 할 것이다.
Notes
Conflicts of Interest
None